Hyperthermie et Cancer : La Chaleur Combat le Cancer [Études 2026]
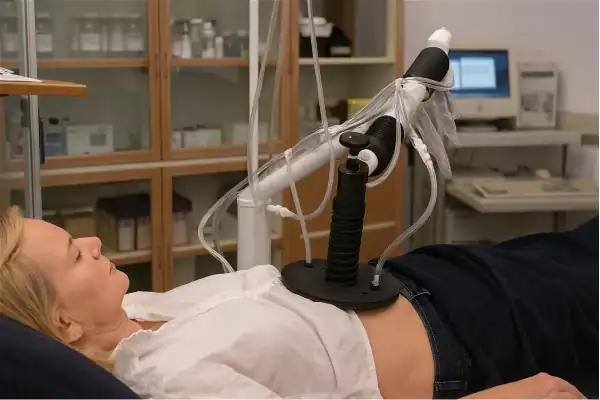
L'hyperthermie, ou thérapie par la chaleur, connaît un regain d'intérêt spectaculaire dans le traitement du cancer. Les recherches 2024-2025 révèlent que cette approche millénaire, combinée aux thérapies conventionnelles, améliore significativement les résultats pour les patients atteints de cancers agressifs.
De la HIPEC (chimiothérapie chauffée intra-péritonéale) à la technologie HEATT® (hyperthermie extracorporelle corps entier), en passant par les saunas infrarouges comme soutien complémentaire, la chaleur s'impose comme un outil thérapeutique puissant dans l'arsenal oncologique moderne.
Sommaire
- L'hyperthermie en oncologie : définition et principes
- Ce que disent les études scientifiques 2024-2025
- Comment la chaleur combat le cancer
- Les 3 types d'hyperthermie médicale
- Protocoles médicaux : HIPEC, HEATT®, radiofréquence
- Approches complémentaires naturelles
- Synergies avec chimiothérapie et immunothérapie
- Précautions et contre-indications
- Questions fréquentes
- Sources scientifiques
L'hyperthermie en oncologie : définition et principes
L'hyperthermie thérapeutique est une technique médicale qui consiste à élever la température des tissus au-dessus de la valeur physiologique normale (37°C) dans un but thérapeutique. En oncologie, cette élévation contrôlée (généralement entre 40 et 45°C) vise à endommager sélectivement les cellules cancéreuses tout en préservant les tissus sains.
🌡️ Pourquoi les cellules cancéreuses sont-elles plus sensibles à la chaleur ?
Cette vulnérabilité s'explique par plusieurs caractéristiques biologiques propres aux tumeurs :
- Vascularisation anarchique : les vaisseaux sanguins tumoraux sont désorganisés et inefficaces pour dissiper la chaleur
- Microenvironnement acide : le pH bas des tumeurs augmente la sensibilité thermique
- Stress oxydatif préexistant : les cellules cancéreuses sont déjà en état de stress métabolique
- Déficiences en protéines de choc thermique (HSP) : capacité réduite à se protéger contre les dommages thermiques
Cette différence de sensibilité permet une "fenêtre thérapeutique" où la chaleur affecte préférentiellement les cellules tumorales.
Ce que disent les études scientifiques (2024-2025)
HIPEC pour le cancer de l'ovaire : amélioration de 50% de la survie
Une étude de cohorte publiée en 2024 dans Gynecologic Oncology portant sur 584 patientes atteintes de cancer de l'ovaire avancé (suivi médian de 42,2 mois) a démontré des résultats remarquables :
- Survie globale médiane : 49,8 mois avec HIPEC vs 34,0 mois sans HIPEC
- Taux de survie à 3 ans : 60,3% vs 49,5%
- Taux de survie à 5 ans : 42,1% vs 31,8%
- Pas d'augmentation significative des effets secondaires graves
Note : L'HIPEC (Hyperthermic Intraperitoneal Chemotherapy) combine chirurgie cytoréductive et perfusion de chimiothérapie chauffée directement dans l'abdomen.
HEATT® : hyperthermie corps entier révolutionnaire
La technologie HEATT® (Hyperthermic Extracorporeal Applied Tumor Therapy), approuvée par la FDA, représente une avancée majeure. Les essais cliniques de phase I/II montrent :
- Cancer du poumon avancé : augmentation significative de la survie par rapport aux témoins
- Cancer de l'ovaire réfractaire : prolongation de la survie chez des patientes en échec thérapeutique
- Maintien précis à 42°C pendant 120 minutes dans tout le corps
- Atteinte des zones difficiles : cerveau, moelle osseuse, métastases multiples
Cette technologie permet de traiter des cancers métastatiques avec une approche systémique.
Synergie hyperthermie + immunothérapie : transformation des tumeurs "froides"
Une revue de 2024 dans Frontiers in Immunology révèle que l'hyperthermie transforme les tumeurs immunologiquement "froides" (peu réactives) en tumeurs "chaudes" (hautement immunogènes) :
- Augmentation de l'expression de PD-L1 sur les cellules tumorales
- Recrutement accru de lymphocytes T CD8+ dans la tumeur
- Libération d'antigènes tumoraux stimulant la réponse immune systémique
- Amélioration de l'efficacité des inhibiteurs de points de contrôle immunitaires
Cette synergie représente l'une des avancées les plus prometteuses en oncologie moderne.
Comment la chaleur combat le cancer
Les recherches moléculaires récentes ont identifié cinq mécanismes principaux expliquant l'efficacité anticancéreuse de l'hyperthermie :
Dénaturation protéique
La chaleur dénature les protéines essentielles au fonctionnement des cellules cancéreuses, perturbant leur homéostasie et déclenchant l'apoptose.
Activation immunitaire
La chaleur provoque une mort cellulaire immunogène, libérant des antigènes tumoraux qui stimulent la réponse immunitaire systémique.
Sensibilisation aux traitements
L'hyperthermie augmente la perméabilité vasculaire tumorale, améliorant la pénétration des médicaments chimiothérapeutiques de 50 à 200%.
Inhibition de la réparation de l'ADN
La chaleur inhibe les enzymes de réparation de l'ADN (comme BRCA2), empêchant les cellules cancéreuses de réparer les dommages causés par la radiothérapie et la chimiothérapie.
Normalisation vasculaire
L'hyperthermie modérée normalise temporairement la vascularisation tumorale, améliorant l'oxygénation et rendant les cellules plus sensibles à la radiothérapie.
🔥 Le rôle clé des protéines de choc thermique (HSP)
Les Heat Shock Proteins (HSP) sont des protéines produites par les cellules en réponse au stress thermique. Elles jouent un rôle ambivalent dans le cancer :
- Effet protecteur initial : les HSP aident les cellules à survivre au stress thermique
- Cible thérapeutique : l'inhibition des HSP (par des molécules comme le 6-shogaol du gingembre) potentialise l'efficacité de l'hyperthermie
- Vecteurs d'antigènes : les HSP peuvent présenter des antigènes tumoraux au système immunitaire
- Biomarqueurs : les niveaux de HSP70/90 peuvent prédire la réponse à l'hyperthermie
Les 3 types d'hyperthermie médicale
| Type | Zone traitée | Température | Durée | Applications principales |
|---|---|---|---|---|
| Locale | Tumeur spécifique | 42-45°C | 30-90 min | Mélanomes, cancers de la peau, tumeurs superficielles |
| Régionale | Organe ou cavité corporelle | 40-43°C | 45-120 min | Cancers pelviens (HIPEC), sarcome des tissus mous, vessie |
| Corps entier | Tout le corps | 39-42°C | 60-180 min | Cancers métastatiques, lymphomes, leucémies (HEATT®) |
⚡ Techniques de chauffage
- Radiofréquence : ondes électromagnétiques pour chauffer localement
- Micro-ondes : chauffage plus profond (jusqu'à 5 cm)
- Ultrasons focalisés (HIFU) : très précis, non invasif
- Infrarouge : saunas thérapeutiques
- Perfusion de liquides chauds : HIPEC, perfusion pleurale
- Extracorporelle : HEATT®, sang chauffé hors du corps
🎯 Cibles oncologiques principales
- Carcinome péritonéal : réponse exceptionnelle à l'HIPEC
- Cancer du col de l'utérus : amélioration de la radiothérapie
- Mélanome : hyperthermie locale combinée à l'immunothérapie
- Cancer du sein localement avancé : néoadjuvant avant chirurgie
- Récidives : option pour les tumeurs résistantes
- Métastases cérébrales : techniques focalisées (HIFU)
Protocoles médicaux : HIPEC, HEATT®, radiofréquence
🏥 HIPEC : Chimiothérapie Hyperthermique Intra-Péritonéale
Procédure : Après résection chirurgicale complète des tumeurs visibles, une solution de chimiothérapie chauffée à 41-43°C est perfusée dans la cavité abdominale pendant 60-90 minutes.
Avantages :
- Concentration locale élevée de chimiothérapie (20-1000× supérieure à la voie intraveineuse)
- Effet synergique chaleur + médicaments
- Réduction de la toxicité systémique
- Élimination des micrométastases résiduelles
Résultats 2024 : Survie médiane augmentée de 15,8 mois dans le cancer de l'ovaire, avec des taux de réponse complets allant jusqu'à 80% dans certains sous-groupes.
💉 HEATT® : Hyperthermie Extracorporelle Corps Entier
Innovation technique : Le sang est prélevé, chauffé à l'extérieur du corps via un échangeur thermique, puis réinjecté. Permet d'atteindre 42°C dans tout l'organisme.
Applications uniques :
- Tumeurs solides métastatiques
- Lymphomes réfractaires
- Leucémies en échec thérapeutique
- Métastases cérébrales (traversée de la barrière hémato-encéphalique)
Protocole type : 8-12 séances de 2 heures, combinées à une chimiothérapie à faible dose ou à une immunothérapie. Surveillance cardiaque et neurologique continue.
📡 Radiofréquence et Micro-ondes : Hyperthermie Focalisée
Principes : Utilisation d'ondes électromagnétiques pour chauffer sélectivement une tumeur. Des électrodes sont placées autour ou à l'intérieur de la lésion.
Avancées 2025 :
- Nanoparticules magnétiques : injectées dans la tumeur, chauffées par champ magnétique externe
- Nanoparticules d'or : absorbent la lumière infrarouge pour un chauffage très localisé
- HIFU guidé par IRM : ultrasons focalisés sous contrôle d'imagerie par résonance magnétique
- Thermothérapie interstitielle laser : fibres optiques implantées dans la tumeur
Indications émergentes : Cancer de la prostate localisé, tumeurs du pancréas non résécables, métastases osseuses douloureuses.
Approches complémentaires naturelles
🌿 Sauna Infrarouge Lointain : Soutien Intégratif
Bénéfices documentés :
- Détoxification profonde : élimination des métaux lourds, pesticides, toxines stockées
- Réduction de la douleur et fatigue : rapportée par 70% des patients en étude observationnelle
- Stimulation immunitaire : augmentation des lymphocytes NK (Natural Killer)
- Amélioration de la circulation : vasodilatation, meilleure oxygénation tissulaire
- Réduction du stress : diminution du cortisol, hormone associée à la progression tumorale
Protocole recommandé (sous supervision médicale) :
- Fréquence : 3-5 séances par semaine
- Durée : 30-45 minutes par séance
- Température : 50-60°C (inférieur au sauna traditionnel)
- Hydratation : 500 ml d'eau avant et après
- Progression : commencer par 20 minutes, augmenter graduellement
🛁 Bains Thermiques Thérapeutiques
Protocole :
- Température : 40-42°C (104-108°F)
- Durée : 20-30 minutes d'immersion
- Ajout : 1-2 tasses de sel d'Epsom (sulfate de magnésium)
- Post-bain : s'envelopper 10-15 minutes pour transpirer
Précautions :
- Eau filtrée sans chlore ni fluorure
- Hydratation abondante
- Arrêt immédiat en cas de vertiges
- Éviter après repas copieux
☀️ Héliothérapie Modérée
Bénéfices combinés chaleur + vitamine D :
- Production de vitamine D (cruciale pour l'immunité anti-cancéreuse)
- Réduction de 40% de la fréquence des infections
- Stimulation du système lymphatique
- Amélioration de l'humeur et du sommeil
Protocole prudent :
- 15-20 minutes par jour (sans écran solaire pour la vitamine D)
- Heures optimales : 10h-15h (UVB maximum)
- Exposition de 45% de la surface corporelle
- Après 20 minutes : écran solaire ou ombre
💊 Composés Naturels Potentialisateurs
Curcumine : Potentialise l'apoptose induite par la chaleur, inhibe HSP70/90, améliore la radiosensibilité. Dose étudiée : 500-1000 mg/jour (avec pipérine pour absorption).
6-Shogaol (gingembre) : Étude 2025 montrant une modulation synergique des ROS et HSP avec l'hyperthermie. Dose : 250-500 mg d'extrait standardisé.
EGCG (thé vert) : Sensibilise les cellules cancéreuses à l'hyperthermie, potentialise les dommages à l'ADN. Dose : 300-600 mg d'extrait décaféiné.
Quercétine : Inhibe HSP70, augmente l'efficacité de l'hyperthermie locale. Dose : 500-1000 mg/jour.
Synergies avec chimiothérapie et immunothérapie
| Combinaison | Mécanisme synergique | Amélioration d'efficacité | Cancers cibles |
|---|---|---|---|
| Hyperthermie + Cisplatine | Augmentation de la formation d'adduits ADN-platine | 50-200% | Ovaire, testicule, poumon |
| Hyperthermie + Doxorubicine | Meilleure pénétration tumorale, inhibition P-glycoprotéine | 30-100% | Sein, sarcomes, lymphomes |
| Hyperthermie + Radiothérapie | Radiosensibilisation, correction de l'hypoxie | Facteur 1.2-1.5 (TER) | Tête et cou, col utérin, rectum |
| Hyperthermie + Anti-PD-1/PD-L1 | Transformation tumeur "froide" en "chaude" | Réponse 40% vs 20% | Mélanome, poumon, vessie |
| Hyperthermie + CAR-T cells | Amélioration de l'infiltration des lymphocytes T | Études précliniques prometteuses | Leucémies, lymphomes réfractaires |
🔄 Mécanismes des synergies documentées
1. Perméabilisation membranaire : La chaleur augmente la fluidité des membranes cellulaires, facilitant l'entrée des médicaments chimiothérapeutiques.
2. Inhibition des pompes d'efflux : L'hyperthermie inhibe les P-glycoprotéines (P-gp) qui expulsent les médicaments des cellules cancéreuses, surmontant ainsi la multi-résistance.
3. Radiosensibilisation : La chaleur potentialise les dommages à l'ADN causés par les radiations et inhibe leur réparation.
4. Immunomodulation : L'hyperthermie libère des antigènes tumoraux, active les cellules dendritiques et recrute des lymphocytes T, créant un environnement propice à l'immunothérapie.
5. Normalisation vasculaire : Une hyperthermie modérée (40-41°C) améliore temporairement la perfusion tumorale, augmentant la délivrance d'oxygène et de médicaments.
Précautions et contre-indications
⚠️ CONTRE-INDICATIONS ABSOLUES À L'HYPERTHERMIE MÉDICALE
- Insuffisance cardiaque sévère (classe NYHA III-IV)
- Maladies cardiovasculaires instables (infarctus récent, angor instable)
- Thrombose veineuse profonde évolutive
- Troubles de la coagulation sévères non contrôlés
- Grossesse (sauf indications vitales exceptionnelles)
- Implants métalliques non compatibles (pour hyperthermie par radiofréquence)
- Pacemaker ou défibrillateur (sauf modèles spécifiquement testés)
- Brûlures étendues ou lésions cutanées sévères dans la zone de traitement
- Incapacité à réguler la température corporelle (lésions hypothalamiques, anhidrose)
Précautions d'usage
⚠️ Attention particulière :
- Neuropathie périphérique : risque de brûlures par défaut de sensation
- Lymphœdème : la chaleur peut temporairement aggraver l'œdème
- Métastases cérébrales : consultation neurologique obligatoire
- Insuffisance rénale : surveillance accrue de l'hydratation
- Traitement par bêta-bloquants : altération de la thermorégulation
- Âge avancé : tolérance réduite, progression plus lente
Sécurité générale
✅ Bien toléré avec précautions :
- Techniques modernes avec monitoring continu
- Équipes médicales spécialisées et formées
- Protocoles standardisés selon les recommandations internationales
- Effets secondaires généralement transitoires : rougeurs, fatigue, légère hyperthermie
- Complications graves exceptionnelles sous surveillance appropriée
Questions fréquentes
- HIPEC : généralement 1 séance pendant la chirurgie
- Hyperthermie locale/radiothérapie : 5-10 séances, 1-2 fois par semaine
- HEATT® (corps entier) : 8-12 séances sur 4-6 semaines
- Sauna infrarouge (soutien) : 3-5 séances par semaine en continu
- HIPEC pour cancer de l'ovaire : remboursée depuis 2019
- Hyperthermie + radiothérapie pour récidives : prise en charge hospitalière
- Hyperthermie corps entier (HEATT®) : protocoles de recherche ou accès compassionnel
- HIPEC : Institut Gustave Roussy (Villejuif), CHU Lyon, CHU Bordeaux, AP-HP Paris
- Hyperthermie locale + radiothérapie : la plupart des centres de radiothérapie oncologique
- Recherche HEATT® : protocoles en cours dans quelques centres spécialisés
- Médecine intégrative : certains centres proposent des saunas infrarouges comme soutien
Sources scientifiques
- Yang KL, et al. (2025). Phase II clinical trial assessing the addition of hyperthermia to salvage concurrent chemoradiotherapy for unresectable recurrent head and neck cancer in previously irradiated patients. Radiation Oncology, 20:21. doi: 10.1186/s13014-025-02585-z
- Abreu MM, Chocron AF, Smadja DM. (2025). From cold to hot: mechanisms of hyperthermia in modulating tumor immunology for enhanced immunotherapy. Frontiers in Immunology, 16:1487296. doi: 10.3389/fimmu.2025.1487296
- Ahn CR, Baek SH. (2025). Synergistic effects of 6-shogaol and hyperthermia on ACHN renal cancer cells: modulation of ROS and heat shock proteins in cancer therapy. Frontiers in Pharmacology, 16:1522285. doi: 10.3389/fphar.2025.1522285
- Szwed M, et al. (2025). Pt-Au Nanoparticles in Combination with Near-Infrared-Based Hyperthermia Increase the Temperature and Impact on the Viability and Immune Phenotype of Human Hepatocellular Carcinoma Cells. International Journal of Molecular Sciences, 26(4):1574. doi: 10.3390/ijms26041574
- Lukácsi S, Munkácsy G, Győrffy B. (2024). Harnessing Hyperthermia: Molecular, Cellular, and Immunological Insights for Enhanced Anticancer Therapies. Integrative Cancer Therapies, 23:15347354241242094. doi: 10.1177/15347354241242094
- Righini MF, Durham A, Tsoutsou PG. (2024). Hyperthermia combined with immune checkpoint inhibitor therapy: Synergistic sensitization and clinical outcomes. Frontiers in Oncology, 14:1428065. doi: 10.3389/fonc.2024.1428065
- Ahn CR, et al. (2024). Hyperthermia Treatment as a Promising Anti-Cancer Strategy: Therapeutic Targets, Perspective Mechanisms and Synergistic Combinations in Experimental Approaches. Antioxidants (Basel), 13(5):564. doi: 10.3390/antiox13050564
- Logghe T, et al. (2024). Hyperthermia in Combination with Emerging Targeted and Immunotherapies as a New Approach in Cancer Treatment. Cancers, 16(3):505. doi: 10.3390/cancers16030505
- Laukkanen JA, Kunutsor SK. (2024). The multifaceted benefits of passive heat therapies for extending the healthspan: A comprehensive review with a focus on Finnish sauna. Temperature (Austin), 11(1):27-51. doi: 10.1080/23328940.2023.2300623
- Kwon S, Jung S, Baek SH. (2023). Combination Therapy of Radiation and Hyperthermia, Focusing on the Synergistic Anti-Cancer Effects and Research Trends. Antioxidants (Basel), 12(4):924. doi: 10.3390/antiox12040924
- Datta NR, et al. (2022). Hyperthermia: A Potential Game-Changer in the Management of Cancers in Low-Middle-Income Group Countries. Integrative Cancer Therapies, 21:15347354211072308.
- van Rhoon GC. (2021). Hyperthermia-Based Anti-Cancer Treatments. Cancers, 13(6):1240. doi: 10.3390/cancers13061240
- Elming PB, et al. (2019). Hyperthermia: The Optimal Treatment to Overcome Radiation Resistant Hypoxia. Cancers, 11(1):60. doi: 10.3390/cancers11010060
- Ishibashi J, et al. (2008). The effects inhibiting the proliferation of cancer cells by far-infrared radiation (FIR) are controlled by the basal expression level of heat shock protein (HSP) 70A. Medical Oncology, 25(2):229-237.
Références issues d'articles évalués par les pairs, essais cliniques et revues systématiques.
En conclusion
L'hyperthermie représente une modalité thérapeutique scientifiquement validée qui connaît un renouveau spectaculaire en oncologie moderne. Les recherches 2024-2025 confirment son rôle comme adjuvant puissant aux traitements conventionnels, avec des mécanismes d'action précis et mesurables.
Des technologies innovantes comme HEATT® pour l'hyperthermie corps entier, l'HIPEC pour les cancers péritonéaux, et les synergies avec l'immunothérapie ouvrent de nouvelles perspectives pour les patients atteints de cancers avancés ou réfractaires.
À retenir : L'hyperthermie médicale doit toujours être pratiquée sous supervision spécialisée dans le cadre d'une stratégie oncologique personnalisée. Les approches complémentaires naturelles (sauna, bains thermiques) peuvent offrir un soutien valuable mais ne remplacent jamais les traitements médicaux. Consultez systématiquement votre oncologue pour une approche adaptée à votre situation spécifique.