Je suis très inquiète parce que j’ai fait des analyses de sang et les résultats du labo, indiquent un taux élevé de 13 % d’éosinophiles alors que tout le reste est ok.
J’ai peur parce que je me sens dernièrement un peu fatiguée.
Est-ce que ce résultat est l’indice d’une maladie latente grave ?
Qu’est-ce que cela signifie ?
Éosinopénie et Éosinophilie Définition
Qu’est-ce que l’éosinophilie ? L‘éosinophilie ou hyperéosinophilie (HE) est une condition dans laquelle le nombre de polynucléaires éosinophiles dans le sang augmente de plus de 0,45 x 109/l (450/µl). La moyenne se situe à 0,125 x 109/l d’éosinophiles chez l’adulte et à 0,225 x 109/l chez l’enfant. Ces cellules sanguines représentent de 2 à 5% des leucocytes circulants. L‘éosinopénie est au contraire une diminution du nombre des éosinophiles. L’éosinophilie est diagnostiquée en faisant la numération formule sanguine complète.
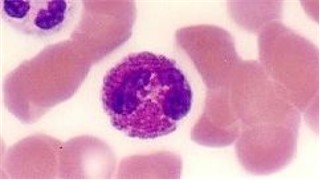
Les éosinophiles sont des globules blancs très présents dans les tissus (peau, poumon, tube digestif, etc.) qui sont produites dans la moelle osseuse. On les appelle ‘polynucléaires’ parce que ces cellules possèdent habituellement un noyau à deux lobes. Sur un frottis sanguin, on identifie facilement les éosinophiles car leur cytoplasme est rempli d’une granulation volumineuse qui se colore en rouge orangé vif (colorables par l’éosine).
Les globules blancs éosinophiles sont impliqués dans le système immunitaire afin d’aider le corps à combattre certaines infections ou allergies et dans le processus de lutte contre les envahisseurs, conduisant à un processus inflammatoire dans le corps. Les éosinophiles possèdent une capacité de phagocytose c’est-à-dire qu’ils emprisonnent des particules étrangères avant de les digérer. Le nombre d’éosinophiles devient élevé en réponse à l’invasion ou aux allergènes.
Les Causes d’un Taux Élevé d’Éosinophiles – Éosinophilie et Pathologies
Il existe plusieurs maladies sous-jacentes qui peuvent provoquer une augmentation des globules blancs polynucléaires éosinophiles. Le nombre des éosinophiles peut être élevé dans les pathologies suivantes:
1. Manifestations allergiques atopiques : Asthme, eczéma, pollinose, rhinites et conjonctivites.
2. Allergie alimentaire : Dermatose prurigineuse, urticaire, etc.
3. Allergies médicamenteuses et utilisation chronique de certains médicaments : Anti-inflammatoires non stéroïdiens (AINS), aspirine, antiépileptiques, héparine, nitrofuranes (Ercéfuryl ®), psychotropes (imipramine, phénothiazines), rifampicine (Rifadine® et Rimactan®), sulfamides (Bactrim®), sels d’or (Ridauran®), allopurinol (Zyloric®), la vitamine B12. En réalité, tous les médicaments peuvent être incriminés dans le cas d’une éosinophilie d’origine médicamenteuse.
4. Infections parasitaires : Ankylostomose (ankylostomes), ascaridiase (ascaris), anguillulose (anguillules), distomatose (douves), bilharziose (schistosomes), filariose (filaires), hydatidose (équinocoques), oxyurose (oxyures), taeniase (tænias), toxocarose (toxocara canis), trichinose (trichine), trichocéphalose (trichocéphale).
5. Autres type d’infections : Infection bactérienne (brucellose et scarlatine), infection fongique (aspergillose et coccidioïdomycose).
6. Certains cancers : Lymphome de Hodgkin ou non hodgkinien, certaines leucémies. En particulier : cancer du sein, du foie, du rein et de la thyroïde.
7. Maladies auto-immunes et inflammatoires : Dermatite herpétiforme, lupus érythémateux systémique (SLE), maladies de Crohn, maladie de Whipple, pemphigus, périartérite noueuse, polyarthrite rhumatoïde, psoriasis et sarcoïdose, syndrome de Churg-Strauss (vascularite systémique) et syndrome de Gougerot Sjögren. Le syndrome hyperéosinophilique idiopathique [SHE] est un syndrome qui concerne surtout les sujets jeunes, le plus souvent masculins.
8. Autres pathologies : Infection par le VIH, insuffisance surrénale, hépatite chronique, pneumonie chronique idiopathique à éosinophiles.
Les symptômes de l’Éosinophilie – Signes de la Hausse d’Éosinophiles
Quels sont les symptômes d’une éosinophilie ? Les symptômes d’éosinophilie sont ceux de l’affection sous-jacente. Par exemple, si le nombre d’éosinophile est élevé à cause de l’asthme, les symptômes se manifesteront par de l’essoufflement, une respiration sifflante et une sensation d’oppression dans la poitrine. Dans la situation d’une éosinophilie due à une infection parasitaire, les symptômes débuteront par des douleurs abdominales, de la fièvre, une diarrhée, de la toux, etc.
Les réactions aux médicaments ont aussi tendance à provoquer des éruptions cutanées et apparaissent après avoir pris un nouveau médicament. Plus rarement, les symptômes associés à une éosinophilie peuvent se manifester par une perte de poids, des sueurs nocturnes, une augmentation du volume des ganglions lymphatiques ou la perte de sensibilité localisée de la peau ou encore des picotements (fourmis) due à une lésion nerveuse.
Que Peux Faire Le Docteur ?
Une fois le diagnostic posé, le médecin cherchera à déterminer la cause de l’éosinophilie. Il peut procéder à des tests cutanés, au dosage des IgE spécifiques ou à des tests multi-allergéniques de dépistage pour confirmer des allergies spécifiques comme celles aux acariens, au pollen, aux moisissures ou à la poussière.
Le docteur peut aussi découvrir l’existence d’une infestation parasitaire grâce à l’analyse d’échantillons de sang et de selles. Aussi, il vous demandera si vous prenez des médicaments nouveaux puisque l’éosinophilie peut être le résultat d’un effet secondaire dudit médicament. Un chien à la maison peut être à l’origine d’une helminthiase appelée ‘toxocarose’ (Toxocara canis ou larva migrans).
Si le médecin ne peut pas déceler la cause de l’éosinophilie, et si elle est légère, il peut demander à revérifier le décompte des polynucléaires éosinophiles six mois plus tard.
Traitement Conventionnel de l’Éosinophilie
Le traitement d’une augmentation anormale des globules blancs éosinophiles consistera à viser la cause de la maladie sous-jacente : soit une allergie, une réaction à un médicament ou une infestation parasitaire. Dans la plupart des cas, les corticostéroïdes à usage local (inhalation, topique) ou à usage systémique (orale, intramusculaire, intraveineuse) sont prescrits afin de contrôler l’allergie et l’inflammation locale. Ces médicaments dits corticoïdes, dérivés de la cortisone, permettent aussi de réduire le nombre d’éosinophiles.
Remèdes Naturels de l’Éosinophilie – Traitement Ayurvédique
Selon la médecine ayurvédique, originaire d’Inde, met l’accent sur la modification de la réponse immunitaire plutôt que sur la suppression de l’immunité.
Un traitement conventionnel par les stéroïdes (médicament immunosuppresseur qui empêche la réponse immunitaire de l’organisme) peut s’avérer fatale dans certains cas d’éosinophilie, surtout quand le taux élevé de polynucléaires éosinophiles est dû à une invasion parasitaire.
1) Curcuma
L’un des meilleurs suppléments naturels ayant des propriétés anti-inflammatoires, analgésiques, antiallergiques est le curcuma. L’administration orale de capsules de curcumine (500 mg) aux effets immunomodulateurs, est bénéfique pour traiter une éosinophilie causée par l’asthme, les allergies et autres réactions inflammatoires.
2) Tulsi
Un autre meilleur remède ayurvédique pour traiter naturellement l’éosinophilie est le Tulsi ou basilic sacré (Ocimum sanctum). Le Tulsi est surtout connu pour ses propriétés antivirales, antibactériennes, antiseptiques, antiasthmatiques, immunomodulatrices et antiallergiques.